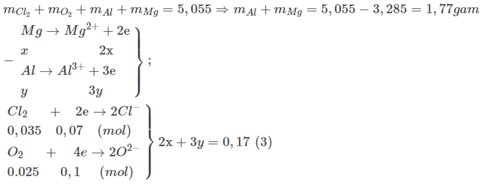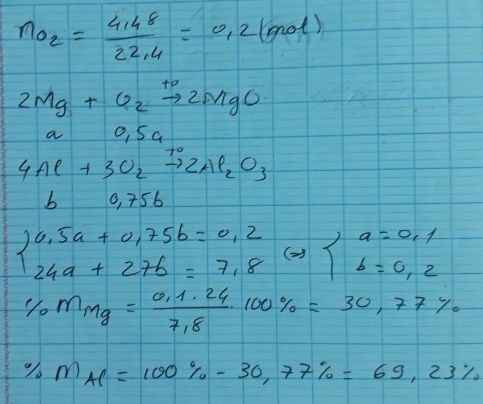Bài 1: Cho 6,72 lít hỗn hợp gồm oxi và clo (đktc) phan ứng vừa đủ với hỗn hợp rắn gồm 0,1 mol Mg và 0,2 mol Al. Tính % về khối lượng của oxi trong hỗn hợp ban đầu
Bài 2: Cho 7,8g hỗn hợp X gồm Mg và Al tác dụng vừa đủ với 5,6 lít hỗn hợp khí Y (đktc) gồm Cl2 và O2 thu được 19,7g hỗn hợp Z gồm 4 chất. Tính %V của O2 trong hỗn hợp Y